Actualización sobre Manejo de la Obesidad 2025-2026
El manejo de la obesidad ha experimentado una transformación paradigmática con la llegada de agonistas de receptores GLP-1 y co-agonistas duales/triples que logran pérdidas de peso de 15-24%, umbrales más bajos para cirugía bariátrica (IMC ≥30 con comorbilidades metabólicas), y evidencia robusta de beneficios cardiovasculares independientes de la pérdida de peso.[1][2][3]
Marco Conceptual: Obesidad como Enfermedad Crónica
La obesidad afecta aproximadamente 42% de adultos en Estados Unidos y está asociada con tasas aumentadas de diabetes tipo 2, hipertensión, enfermedad cardiovascular, trastornos del sueño, osteoartritis y muerte prematura.[1] El tratamiento basado en evidencia combina intervenciones en cinco categorías principales: intervenciones conductuales, nutrición, actividad física, farmacoterapia y procedimientos metabólicos/bariátricos.[1] Figure 1 5A Framework (Assess, Advise, Agree, Assist, Arrange) for Obesity Counseling in the Outpatient Setting undefined
Figure 1 5A Framework (Assess, Advise, Agree, Assist, Arrange) for Obesity Counseling in the Outpatient Setting undefined
Un principio fundamental es que la obesidad requiere tratamiento de por vida, similar a otras condiciones metabólicas crónicas. El monitoreo frecuente del logro de metas de tratamiento y evitar la inercia terapéutica ajustando o intensificando el tratamiento cuando sea necesario son marcos esenciales.[4]
Medicamentos para Obesidad: Eficacia y Seguridad
Agonistas GLP-1 y co-agonistas: Nueva era farmacológica
Actualmente, seis medicamentos están aprobados por la FDA para uso a largo plazo: agonistas del receptor GLP-1 (semaglutida y liraglutida), tirzepatida (agonista dual GIP/GLP-1), fentermina-topiramato, naltrexona-bupropión y orlistat.[1][2] De estos, tirzepatida tiene el mayor efecto, con pérdida de peso promedio de 21% a las 72 semanas.[1] Figure 2 Percentage of Adults With Obesity Without Diabetes Achieving Specific Weight-Loss Targets by Antiobesity Medication Gudzune KA, Kushner RF. Medications for Obesity: A Review. Jama. 2024;332(7):571-584. doi:10.1001/jama.2024.10816.
Figure 2 Percentage of Adults With Obesity Without Diabetes Achieving Specific Weight-Loss Targets by Antiobesity Medication Gudzune KA, Kushner RF. Medications for Obesity: A Review. Jama. 2024;332(7):571-584. doi:10.1001/jama.2024.10816.  Table 2 Coprimary, Confirmatory, and Selected Supportive Secondary and Exploratory End Points for the Treatment Policy Estimand.* Wilding JPH, Batterham RL, Calanna S, et al. Once-Weekly Semaglutide in Adults With Overweight or Obesity. The New England Journal of Medicine. 2021;384(11):989-1002. doi:10.1056/NEJMoa2032183.
Table 2 Coprimary, Confirmatory, and Selected Supportive Secondary and Exploratory End Points for the Treatment Policy Estimand.* Wilding JPH, Batterham RL, Calanna S, et al. Once-Weekly Semaglutide in Adults With Overweight or Obesity. The New England Journal of Medicine. 2021;384(11):989-1002. doi:10.1056/NEJMoa2032183.
Una revisión sistemática de 2025 que incluyó 26 ensayos clínicos aleatorizados con 15,491 participantes demostró que, comparado con placebo:[7]
- Tirzepatida 15 mg semanal: pérdida de peso hasta 17.8% (IC 95%, 16.3% a 19.3%) después de 72 semanas
- Semaglutida 2.4 mg semanal: hasta 13.9% (IC 95%, 11.0% a 16.7%) después de 68 semanas
- Liraglutida 3.0 mg diaria: hasta 5.8% (IC 95%, 3.6% a 8.0%) después de 26 semanas
En ensayos originales de fase 3 para obesidad, la reducción de peso promedio comparada con placebo ha variado de 5.3% a 17.8% después de 56 a 72 semanas, con mejoras en varios riesgos y complicaciones relacionadas con obesidad.[8] En la práctica del mundo real, la eficacia para reducción de peso es frecuentemente menor, por ejemplo, aproximadamente 8% para individuos con diabetes y 11% para individuos sin diabetes a las 60 semanas con semaglutida 2.4 mg/día.[8]
Agentes en desarrollo: Retatrutida
Retatrutida, un agonista triple de receptores GIP/GLP-1/glucagón, produjo pérdida de peso aún mayor de hasta 22.1% (IC 95%, 19.3% a 24.9%) después de 48 semanas en estudios de fase 2.[7] En un ensayo de fase 2 con 338 participantes, retatrutida logró una pérdida de peso promedio de 24.2% para la dosis de 12 mg a las 24 semanas, comparado con 2.1% para placebo.[5] Figure New Molecules and Emerging Indications for GLP-1 Medicines undefined
Figure New Molecules and Emerging Indications for GLP-1 Medicines undefined
El tratamiento con retatrutida resultó en mejoras significativas y clínicamente relevantes en el control glucémico, con reducciones robustas de peso corporal que no parecían haber alcanzado meseta a las 36 semanas.[10] Concurrentemente, retatrutida mejoró el perfil lipídico y redujo la presión arterial, indicando resultados cardiometabólicos generales mejorados.[10]
Perfil de seguridad
Aunque los eventos adversos fueron frecuentes (agonistas GLP-1 vs. placebo: 80% a 97% vs. 63% a 100%), la mayoría fueron relacionados con el tracto gastrointestinal (47% a 84% vs. 13% a 63%, respectivamente), más comúnmente náusea, vómito, diarrea y estreñimiento.[7] Los eventos adversos que requirieron discontinuación del tratamiento (0% a 26% vs. 0% a 9%, respectivamente) y eventos adversos serios (0% a 10% vs. 0% a 12%, respectivamente) fueron raros.[7]
Los efectos adversos de tirzepatida son dosis-dependientes e incluyen comúnmente náusea (25%-29%), diarrea (19%-23%), estreñimiento (11%-17%) y vómito (8%-13%). Estos efectos adversos típicamente ocurren durante el período de escalamiento de dosis y son principalmente de severidad leve a moderada.[5]
Recomendaciones de Guías 2025-2026
Guía conjunta TOS/OMA/OAC 2026
La guía de consenso de expertos 2026 usando el enfoque GRADE emitió recomendaciones fuertes para bupropión-naltrexona, semaglutida, tirzepatida y setmelanotida, con evidencia de certeza moderada.[2] Se hicieron recomendaciones condicionales para otros agentes y complicaciones específicas de obesidad (apnea obstructiva del sueño, insuficiencia cardíaca con fracción de eyección preservada, enfermedad hepática esteatósica asociada a disfunción metabólica, osteoartritis, eventos cardiovasculares adversos mayores y diabetes tipo 2).[2]
Un hallazgo crítico es que continuar los medicamentos para obesidad durante el mantenimiento de peso recibió una recomendación fuerte.[2] Cuando se discontinúa el uso de GLP-1, la recuperación de peso es común; en un estudio de 3,739 participantes, más del 25% recuperó 2% o más de peso en el seguimiento a 2 años.[1] Figure 5 General Overview of Patient’s Weight Management Journey With NuSH Therapies undefined
Figure 5 General Overview of Patient’s Weight Management Journey With NuSH Therapies undefined
Criterios de selección de pacientes
Los medicamentos antiobesidad están recomendados para pacientes no embarazadas con obesidad o sobrepeso y comorbilidades relacionadas con el peso en conjunto con modificaciones del estilo de vida.[1] Las guías AACE 2025 recomiendan considerar farmacoterapia para adultos con IMC ≥30 kg/m² o IMC ≥27 kg/m² con comorbilidades relacionadas con obesidad.[12]
Cirugía Metabólica y Bariátrica
Nuevos umbrales de IMC
Mientras que previamente se limitaba a personas con IMC ≥40 o IMC ≥35 con comorbilidad relacionada con el peso, las guías recientes recomiendan que la cirugía metabólica y bariátrica debe considerarse para pacientes con IMC ≥35 y pacientes con IMC 30-34.9 que tienen enfermedad metabólica concurrente.[1] Umbrales de peso más bajos deben aplicarse a poblaciones asiáticas.[1]
Las guías ASMBS/IFSO 2022 establecen que la cirugía metabólica y bariátrica está recomendada para individuos con IMC >35 kg/m², independientemente de la presencia, ausencia o severidad de comorbilidades.[3] La cirugía debe considerarse para individuos con enfermedad metabólica e IMC de 30-34.9 kg/m².[3] Table UT1 SORT: KEY RECOMMENDATIONS FOR PRACTICE Banerjee ES, Schroeder R, Harrison TD. Metabolic Surgery for Adult Obesity: Common Questions and Answers. American Family Physician. 2022;105(6):593-601.
Table UT1 SORT: KEY RECOMMENDATIONS FOR PRACTICE Banerjee ES, Schroeder R, Harrison TD. Metabolic Surgery for Adult Obesity: Common Questions and Answers. American Family Physician. 2022;105(6):593-601.  Figure 5 Algorithm for the Treatment of Type 2 Diabetes Mellitus, as Suggested by the International Diabetes Organizations Pareek M, Schauer PR, Kaplan LM, et al. Metabolic Surgery: Weight Loss, Diabetes, and Beyond. Journal of the American College of Cardiology. 2018;71(6):670-687. doi:10.1016/j.jacc.2017.12.014.
Figure 5 Algorithm for the Treatment of Type 2 Diabetes Mellitus, as Suggested by the International Diabetes Organizations Pareek M, Schauer PR, Kaplan LM, et al. Metabolic Surgery: Weight Loss, Diabetes, and Beyond. Journal of the American College of Cardiology. 2018;71(6):670-687. doi:10.1016/j.jacc.2017.12.014.
Eficacia y resultados
Dos procedimientos metabólicos y bariátricos comprenden más del 90% de todas las cirugías: gastrectomía en manga laparoscópica (LSG) y bypass gástrico en Y de Roux (RYGB).[1] La pérdida de peso esperada a 12 meses es aproximadamente 25% después de LSG y aproximadamente 30% después de RYGB, con pérdida de peso sostenida a 5 años.[1]
Los ensayos clínicos aleatorizados muestran resultados superiores con cirugía metabólica y bariátrica comparada con intervención de estilo de vida o cuidado usual en peso, factores de riesgo cardiometabólico y resultados de diabetes tipo 2, mientras que estudios observacionales de alta calidad muestran mayor remisión de diabetes tipo 2, menor incidencia de cáncer, reducción de morbilidad y mortalidad cardiovascular, y mortalidad por todas las causas comparado con controles no operados emparejados.[15]
Complicaciones y seguimiento
Las complicaciones tempranas incluyen fugas anastomóticas (LSG: 1%-7%; RYGB: 0.6%-4.4%), estenosis (LSG: 1%-9%; RYGB: 8%-19%), sangrado postoperatorio (11%) y eventos tromboembólicos venosos.[1] Las complicaciones tardías incluyen hernia interna y ulceración marginal (RYGB: 2.5%-5%).[1]
Se recomienda tamizaje y suplementación pre y post-cirugía metabólica y bariátrica para micronutrientes (tiamina, vitamina B12, folato, hierro, vitamina D, calcio, vitamina A, vitamina E, vitamina K, zinc y cobre).[1]
Beneficios Cardiovasculares de los Medicamentos para Obesidad
Evidencia de reducción de eventos cardiovasculares
El estudio SELECT demostró que semaglutida mejoró los resultados cardiovasculares en pacientes con sobrepeso u obesidad y enfermedad cardiovascular establecida sin diabetes.[16] Semaglutida se asoció con una reducción de 20% en eventos cardiovasculares adversos mayores (MACE) comparado con placebo.[16] Figure 6 Weight Loss Induced by SGLT2 Inhibitors and GLP1-RA and MACE/Mortality Després JP, Carpentier AC, Tchernof A, Neeland IJ, Poirier P. Management of Obesity in Cardiovascular Practice: JACC Focus Seminar. Journal of the American College of Cardiology. 2021;78(5):513-531. doi:10.1016/j.jacc.2021.05.035.
Figure 6 Weight Loss Induced by SGLT2 Inhibitors and GLP1-RA and MACE/Mortality Després JP, Carpentier AC, Tchernof A, Neeland IJ, Poirier P. Management of Obesity in Cardiovascular Practice: JACC Focus Seminar. Journal of the American College of Cardiology. 2021;78(5):513-531. doi:10.1016/j.jacc.2021.05.035.  Figure 1 CV Outcomes in Male and Female Subjects Verma S, Colhoun HM, Dicker D, et al. Semaglutide Effects on Cardiovascular Outcomes in People With Overweight or Obesity (SELECT): Outcomes by Sex. Journal of the American College of Cardiology. 2024;84(17):1678-1682. doi:10.1016/j.jacc.2024.08.022.
Figure 1 CV Outcomes in Male and Female Subjects Verma S, Colhoun HM, Dicker D, et al. Semaglutide Effects on Cardiovascular Outcomes in People With Overweight or Obesity (SELECT): Outcomes by Sex. Journal of the American College of Cardiology. 2024;84(17):1678-1682. doi:10.1016/j.jacc.2024.08.022.
Un meta-análisis de 2025 que incluyó 56 ensayos clínicos con 60,307 pacientes encontró que tanto tirzepatida como semaglutida demostraron restauración de normoglucemia, remisión de diabetes tipo 2 y reducción en hospitalización por insuficiencia cardíaca.[19] Semaglutida fue efectiva en reducir eventos cardiovasculares adversos mayores y reducir dolor en osteoartritis de rodilla. Tirzepatida fue efectiva en remisión de síndrome de apnea obstructiva del sueño y esteatohepatitis asociada a disfunción metabólica.[19]
Mecanismos más allá de la pérdida de peso
Los datos son consistentes con que la diferencia entre grupos en la incidencia de enfermedad cardiovascular emerge temprano, lo que sugiere que cambios fisiológicos más rápidos inducidos por el tratamiento más allá de la magnitud de la pérdida de peso corporal pueden haber mediado al menos parte del beneficio cardiovascular.[16]
Los medicamentos de la clase de agonistas del receptor GLP-1 han demostrado en animales con o sin diabetes reducir inflamación, mejorar función endotelial y ventricular izquierda, promover estabilidad de placa y disminuir agregación plaquetaria.[16] Semaglutida se asoció con cambios en múltiples biomarcadores de riesgo cardiovascular, incluyendo presión arterial, circunferencia de cintura, control glucémico, nefropatía y niveles de lípidos y proteína C reactiva.[16]
Consideraciones Nutricionales con Terapia GLP-1
Prevención de deficiencias nutricionales
Los individuos que usan GLP-1 para tratar obesidad experimentan reducciones significativas en apetito e ingesta energética, con reducciones calóricas observadas de 16%-39%.[8] Esta reducción grande y rápida puede llevar a ingestas insuficientes de vitaminas y minerales esenciales, especialmente con ingestas energéticas <1200 kcal/día para mujeres y <1800 kcal/día para hombres.[8]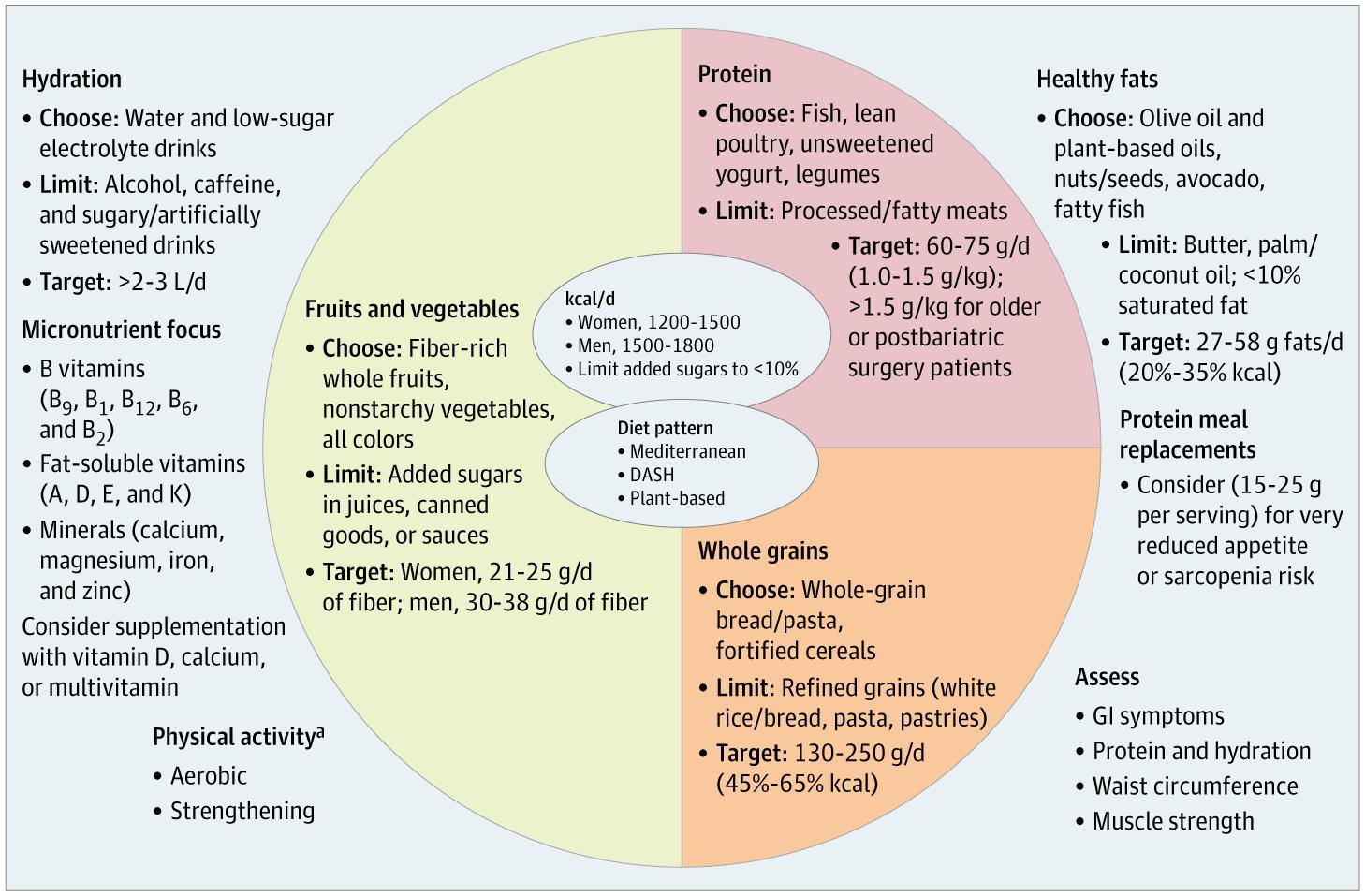 Figure Integrating Nutrition and Physical Activity with GLP-1 and Dual Receptor Agonist Therapy undefined
Figure Integrating Nutrition and Physical Activity with GLP-1 and Dual Receptor Agonist Therapy undefined
La guía dietética para individuos usando GLP-1 debe enfocarse en asegurar adecuación de nutrientes dentro de una dieta frecuentemente sustancialmente más baja en calorías.[8] Los clínicos deben enfatizar una diversidad de alimentos densos en nutrientes, mínimamente procesados como frutas, verduras, granos enteros, legumbres, proteínas magras, nueces y semillas.[8]
Los nutrientes de preocupación incluyen hierro, calcio, magnesio, zinc y vitaminas A, D, E, K, B1, B12 y C.[8] Los suplementos dietéticos pueden considerarse proactivamente para nutrientes en riesgo, como vitamina D, calcio, B12, o una tableta multivitamínica-mineral, en dosis apropiadas y adaptadas a las necesidades de cada persona.[8]
Preservación de masa muscular y ósea
Para individuos con GLP-1, la ingesta adecuada de proteína dietética puede ser difícil de lograr debido a apetito reducido y/o aversiones al sabor.[8] Se deben alentar alimentos ricos en proteína de bajo volumen y densos en nutrientes, como pescado, huevos, yogur griego, queso cottage y nueces/semillas.[8]
Críticamente, los clínicos deben entender—y enfatizar a individuos tomando GLP-1—que el aumento de ingesta de proteína solo es probablemente inadecuado para apoyar la preservación de masa muscular en ausencia de entrenamiento de resistencia/fuerza estructurado.[8] El exceso de proteína dietética, por encima de las necesidades musculares para reparación o crecimiento, puede convertirse en grasa por el hígado y aumentar la adiposidad visceral.[8]
Los programas de entrenamiento de fuerza (resistencia) estructurados o entrenamiento mixto (resistencia más aeróbico) están bien establecidos para ayudar a preservar masa magra durante la reducción de peso.[8] En un ensayo aleatorizado reciente, un año de terapia GLP-1 combinada con entrenamiento de ejercicio preservó la densidad mineral ósea, mientras que la terapia GLP-1 sola disminuyó la densidad mineral ósea.[8]
Consideraciones especiales
Las dietas cetogénicas o muy bajas en carbohidratos pueden ser un enfoque práctico para pérdida de peso y control glucémico para algunas personas. Para individuos con diabetes, la dieta cetogénica en combinación con terapia GLP-1 podría aumentar el riesgo de cetoacidosis diabética e hipoglucemia.[8]
El ayuno intermitente puede aumentar el riesgo de hipoglucemia en individuos con diabetes tipo 2 en agentes hipoglucemiantes. Los individuos en terapia GLP-1 también pueden practicar ayuno intermitente no intencional, debido a no tener hambre. Incluso cuando usan ayuno intermitente, los individuos tomando GLP-1 deben ser alentados a consumir comidas en horarios regulares del día.[8]
Intervenciones de Estilo de Vida
Intervenciones conductuales multicomponente
Todos los pacientes con obesidad (o sobrepeso con anormalidad cardiometabólica) deben ser ofrecidos o referidos a intervenciones conductuales intensivas y multicomponente dentro de atención primaria, entornos comunitarios o a programas comerciales basados en evidencia.[1] Los programas de intensidad moderada a alta incluyen 12 o más sesiones en el primer año (idealmente ≥14 sesiones en 6 meses), seguidas de una fase de mantenimiento hasta 24 meses.[1]
Las intervenciones frecuentemente producen pérdida de peso de 5% a 10% (media, −2.39 kg; IC 95%, −2.86 kg a −1.93 kg), con pérdida máxima lograda entre 6 y 12 meses.[1] La recuperación de peso es común después del cese del programa; en un estudio de 3,739 participantes, más del 25% de participantes recuperó 2% o más de peso en el seguimiento a 2 años.[1]
Actividad física
La actividad física sin reducción calórica típicamente causa menos pérdida de peso (2-3 kg) pero es importante para el mantenimiento de la pérdida de peso.[1] Los programas de entrenamiento de ejercicio estructurados, por ejemplo, 360 minutos/semana con énfasis en ejercicios de fuerza, ayudan a preservar masa libre de grasa.[8]
References
- Obesity Management in Adults: A Review. Elmaleh-Sachs A, Schwartz JL, Bramante CT, et al. JAMA. 2023;330(20):2000-2015. doi:10.1001/jama.2023.19897.
- Joint TOS/OMA/OAC Expert Guidance Statement on the Pharmacological Management of United States Adults With Overweight or Obesity Using the GRADE Approach. Alexander L, Purnell JQ, Burridge K, et al. Obesity (Silver Spring, Md.). 2026;. doi:10.1002/oby.70164.
- 2022 American Society of Metabolic and Bariatric Surgery (ASMBS) and International Federation for the Surgery of Obesity and Metabolic Disorders (IFSO) Indications for Metabolic and Bariatric Surgery. Eisenberg D, Shikora SA, Aarts E, et al. Obesity Surgery. 2023;33(1):3-14. doi:10.1007/s11695-022-06332-1.
- Obesity in Adults. Lingvay I, Cohen RV, Roux CWL, Sumithran P. Lancet (London, England). 2024;404(10456):972-987. doi:10.1016/S0140-6736(24)01210-8.
- Medications for Obesity: A Review. Gudzune KA, Kushner RF. JAMA. 2024;332(7):571-584. doi:10.1001/jama.2024.10816.
- Once-Weekly Semaglutide in Adults with Overweight or Obesity. Wilding JPH, Batterham RL, Calanna S, et al. The New England Journal of Medicine. 2021;384(11):989-1002. doi:10.1056/NEJMoa2032183.
- Efficacy and Safety of Glucagon-Like Peptide-1 Receptor Agonists for Weight Loss Among Adults Without Diabetes : A Systematic Review of Randomized Controlled Trials. Moiz A, Filion KB, Toutounchi H, et al. Annals of Internal Medicine. 2025;178(2):199-217. doi:10.7326/ANNALS-24-01590.
- Nutritional Priorities to Support GLP-1 Therapy for Obesity: A Joint Advisory From the American College of Lifestyle Medicine, the American Society for Nutrition, the Obesity Medicine Association, and the Obesity Society. Mozaffarian D, Agarwal M, Aggarwal M, et al. The American Journal of Clinical Nutrition. 2025;122(1):344-367. doi:10.1016/j.ajcnut.2025.04.023.
- New Molecules and Indications for GLP-1 Medicines. Gonzalez-Rellan MJ, Drucker DJ. JAMA. 2025;334(14):1231-1234. doi:10.1001/jama.2025.14392.
- Retatrutide, a GIP, GLP-1 and Glucagon Receptor Agonist, for People With Type 2 Diabetes: A Randomised, Double-Blind, Placebo and Active-Controlled, Parallel-Group, Phase 2 Trial Conducted in the USA. Rosenstock J, Frias J, Jastreboff AM, et al. Lancet (London, England). 2023;402(10401):529-544. doi:10.1016/S0140-6736(23)01053-X.
- 2025 Concise Clinical Guidance: An ACC Expert Consensus Statement on Medical Weight Management for Optimization of Cardiovascular Health: A Report of the American College of Cardiology Solution Set Oversight Committee. Gilbert O, Gulati M, Gluckman TJ, et al. Journal of the American College of Cardiology. 2025;86(7):536-555. doi:10.1016/j.jacc.2025.05.024.
- American Association of Clinical Endocrinology Consensus Statement: Algorithm for the Evaluation and Treatment of Adults With Obesity/Adiposity-Based Chronic Disease - 2025 Update. Nadolsky K, Garvey WT, Agarwal M, et al. Endocrine Practice : Official Journal of the American College of Endocrinology and the American Association of Clinical Endocrinologists. 2025;31(11):1351-1394. doi:10.1016/j.eprac.2025.07.017.
- Metabolic Surgery for Adult Obesity: Common Questions and Answers. Banerjee ES, Schroeder R, Harrison TD. American Family Physician. 2022;105(6):593-601.
- Metabolic Surgery: Weight Loss, Diabetes, and Beyond. Pareek M, Schauer PR, Kaplan LM, et al. Journal of the American College of Cardiology. 2018;71(6):670-687. doi:10.1016/j.jacc.2017.12.014.
- Approach to Obesity Treatment in Primary Care: A Review. Yanovski SZ, Yanovski JA. JAMA Internal Medicine. 2024;184(7):818-829. doi:10.1001/jamainternmed.2023.8526.
- Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. Lincoff AM, Brown-Frandsen K, Colhoun HM, et al. The New England Journal of Medicine. 2023;389(24):2221-2232. doi:10.1056/NEJMoa2307563.
- Management of Obesity in Cardiovascular Practice: JACC Focus Seminar. Després JP, Carpentier AC, Tchernof A, Neeland IJ, Poirier P. Journal of the American College of Cardiology. 2021;78(5):513-531. doi:10.1016/j.jacc.2021.05.035.
- Semaglutide Effects on Cardiovascular Outcomes in People With Overweight or Obesity (SELECT): Outcomes by Sex. Verma S, Colhoun HM, Dicker D, et al. Journal of the American College of Cardiology. 2024;84(17):1678-1682. doi:10.1016/j.jacc.2024.08.022.
- A Systematic Review and Meta-Analysis of the Efficacy and Safety of Pharmacological Treatments for Obesity in Adults. McGowan B, Ciudin A, Baker JL, et al. Nature Medicine. 2025;:10.1038/s41591-025-03978-z. doi:10.1038/s41591-025-03978-z.
- Integrating Diet and Physical Activity When Prescribing GLP-1s—Lifestyle Factors Remain Crucial. Mehrtash F, Dushay J, Manson JE. JAMA Internal Medicine. 2025;185(9):1151-1152. doi:10.1001/jamainternmed.2025.1794.
